식품의약품안전처와 질병관리청은 코로나19 확진 검사를 위해 지난해 2월 긴급사용 승인한 확진용 유전자진단시약 7개 제품 사용을 종료한다고 4일 밝혔다.
4일부터는 정식허가 제품만 코로나 확진검사에 사용해야 한다.
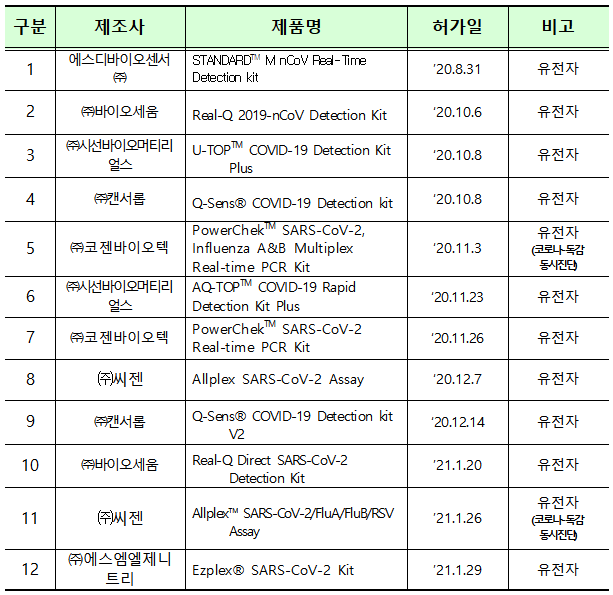
식약처는 확진용 유전자진단시약의 허가현황, 생산량·공급량·재고량 등을 고려할 때 정식허가된 12개 제품이 긴급사용 제품을 대체할 수 있다고 판단했다.
긴급사용은 감염병 대유행이 우려돼 진단시약이 필요하지만 국내에 허가제품이 없을 때 중앙행정기관의 장이 요청한 제품을 한시적으로 제조·판매·사용할 수 있게 하는 특례제도다.
식약처와 질병청은 코로나19 발생 초기에 진단시약 긴급사용을 추진해 확진용 7개 제품을 승인했다.
식약처는 긴급사용 제품의 정식허가 전환을 위해 지난해 4월부터 밀착지원했다. 이에따라 3일 긴급사용을 종료하게 됐다.
질병청은 현장에서 무리없이 긴급사용을 종료하고 정식허가제품을 사용할 수 있도록 긴급사용 제조업체 간담회, 대한진단검사의학회 등을 통해 사전 안내했다.
식약처 관계자는 "정식허가된 12개 제품의 1일 최대 생산량은 64만여명분으로 안정적인 공급과 수급을 이어갈 것"이라며 "코로나 검사에 문제가 되지 않도록 현장모니터링 등을 지속적으로 실시하겠다"고 말했다. ⓒ 세이프타임즈

